Những thập niên gần đây nổi cộm lên vấn đề gia tăng các tác động nhân sinh tới các hệ sinh thái biển do hậu quả ô nhiễm biển và đại dương. Sự lan truyền của nhiều chất ô nhiễm đã đạt tới quy mô địa phương, khu vực và thậm chí toàn cầu. Vì vậy, ô nhiễm các biển, đại dương và sinh giới đã trở thành một vấn đề quốc tế quan trọng nhất và sự tất yếu phải bảo vệ môi trường biển khỏi ô nhiễm là do những yêu cầu sử dụng hợp lý tài nguyên thiên nhiên quy định.
Nhóm liên kết các chuyên gia về những khía cạnh khoa học ô nhiễm biển, trong đó có các chuyên gia Liên Xô, đã hình thành một định nghĩa về ô nhiễm biển được Uỷ ban Hải dương học Liên chính phủ (năm 1967) ủng hộ và Hội nghị của Liên hợp quốc về các vấn đề môi trường tại Stockholm, Thụy Điển (năm 1972) chấp nhận. Ô nhiễm biển được hiểu là: “Tất cả các chất hoặc năng lượng do con người trực tiếp hay gián tiếp đưa vào môi trường biển (kể cả các vùng cửa sông) kéo theo những hậu quả tai hại, như gây thiệt hại tài nguyên sinh vật, nguy hiểm với sức khỏe con người, khó khăn cho hoạt động trên biển (kể cả đánh bắt cá), làm suy thoái chất lượng và giảm các tính chất hữu ích của nước biển”. Danh mục các chất ô nhiễm bao gồm các chất độc, phát thải nước nóng (ô nhiễm nhiệt), vi khuẩn gây bệnh, chất thải rắn, chất lơ lửng, chất dinh dưỡng và một số dạng tác động nhân sinh khác.
Cấp thiết nhất hiện nay là vấn đề ô nhiễm hóa học đại dương.
Thành phần và khối lượng các chất ô nhiễm trong đại dương
Các chất ô nhiễm đại dương và biển xuất phát từ những nguồn sau đây:
- Thải nước công nghiệp và sản xuất trực tiếp vào biển hoặc cùng với nước sông tải ra;
- Nguồn các chất sử dụng trong nông nghiệp và nghề rừng từ lục địa đi vào biển;
- Con người chủ động chôn cất các chất ô nhiễm trong biển;
- Rò rỉ các chất khác trong quá trình hoạt động tầu thủy;
- Phát thải do sự cố từ tầu hoặc ống dẫn dưới nước;
- Khai thác khoáng sản ở đáy biển;
- Vận chuyển các chất ô nhiễm qua khí quyển.
Nhóm các chất ô nhiễm đã phát hiện thấy trong đại dương được liệt kê trong bảng 1.1. Ngoài ra còn có rất nhiều hợp chất hữu cơ, chất thải nhà máy có hàm lượng BOD cao, các phần tử lơ lửng, bằng những con đường khác nhau đi vào đại dương. Như đã thấy, danh mục các chất ô nhiễm mà đại dương nhận thật rất dài. Chúng khác nhau về mức độ độc hại và quy mô phân bố – từ các vùng ven bờ (địa phương) đến toàn cầu.
Bảng 1.2 cho ta khái niệm về độ lớn và tương quan giữa các dòng chất độc hại chính đi vào đại dương, theo số liệu các năm 1985–1986.
Bảng 1.1. Các hợp phần độc hại phổ biến nhất của ô nhiễm vĩ mô
Đại dương Thế giới (Patin, 1979)
| Các chất ô nhiễm | Mức độ nguy hiểm sinh học * | Phạm vi hoạt động |
| Nuclit phóng xạ | Toàn cầu | |
| 90Sr | ,, | |
| 137Cs | ,, | |
| 238Pu | ,, | |
| 3H | ,, | |
| 144Ce | ,, | |
| Hợp chất clo có độc tính | ||
| DDT và các biến thể | ++ | Toàn cầu |
| Policlorbifenil (PCB) | ++ | ,, |
| Aldrin | ++ | ,, |
| Dildrin | ++ | Địa phương |
| Linđan | ++ | ,, |
| Kim loại | ||
| Methyl thủy ngân | ++ | Toàn cầu |
| Cađimi | (+) | ,, |
| Thủy ngân | ++ | ,, |
| Chì | (+) | ,, |
| Đồng | + | Địa phương |
| Kẽm | + | Khu vực |
| Crôm | (-) | Địa phương |
| Mangan | (-) | ,, |
| Asen | (+) | Khu vực |
| Dầu mỏ và sản phẩm dầu | + | Toàn cầu |
| Các chất tẩy | ? | Khu vực |
*) Mức độ nguy hiểm sinh học đối với sinh vật biển: ++ (mạnh), + (đáng kể), (+) (yếu), ? (chưa xác định), (–) (không đáng kể).
Trong Đại dương Thế giới ngày càng thấy nhiều chất ô nhiễm mới. Những chất nguy hiểm nhất đối với cơ thể như các hợp chất hữu cơ chứa clo, hyđrô cacbua thơm mạch vòng và một số chất khác, đang lan truyền ở quy mô toàn cầu. Chúng có khả năng tích tụ cao trong cơ thể sinh vật, độc tính mạnh và gây ung thư.
Bảng 1.2. Tỉ phần nhân sinh (tấn/năm) của một số chất ô nhiễm chính ở Đại dương Thế giới (Izrael, Shiban, 1988)
| Chất ô nhiễm | |||||||
| Dòng | |||||||
| Tự nhiên | Nhân sinh | Tỉ phần dòng nhân sinh trong dòng tổng (%) | |||||
| Dòng vào đại dương | |||||||
| Từ lục địa | Từ không khí | ||||||
| Chì | 1,8.105 | 2,1.106 | 92 | (1-20).105 | (2-20).105 | ||
| Thủy ngân | 3,0.103 | 7,0.103 | 70 | (5-8).103 | (2-3).103 | ||
| Cađimi | 1,7.104 | 1,7.104 | 50 | (1-20).103 | (0,5-4).103 | ||
| Dầu mỏ | 6,0.105 | 4,4.106 | 88 | (3-4).103 | (3-5).103 | ||
| Hyđrô cacbua chứa clo: | |||||||
| PCB | - | 8.103 | 100 | (1-3).103 | (5-7).103 | ||
| Thuốc bảo vệ thực vật, Dibenzodiocxin, Dibenzofuran | - | 1,1.104 | 100 | (4-6).103 | (3-7).103 |
Sự tăng lên không ngừng các tác động tổng hợp của nhiều chất ô nhiễm dẫn đến biến đổi phú dưỡng ngày càng nhanh ở các vùng ven biển và sự ô nhiễm nước do vi sinh vật, gây rất nhiều khó khăn đối với việc dùng nước cho nhu cầu con người.
Dầu mỏ và các sản phẩm dầu
Dầu mỏ là chất lỏng dạng dầu nhớt, thường có màu nâu thẫm và có khả năng phát sát ngoại yếu. Dầu mỏ chủ yếu cấu tạo từ các hyđrô cacbua béo bão hoà và các hyđrô cacbua thơm (từ C5 đến C70) và chứa 80–85 % C, 10–14 % H, 0,01–7 % S, 0,01 % N và 0–7 % O2.
Các thành phần chính của dầu mỏ là hyđrô cacbua (tới 98%) – được chia thành 4 nhóm.
1) Nhóm các chất parafin (Alkane) – thạch lạp (chiếm gần 90 % tổng thành phần của dầu mỏ) và là hợp chất bão hòa bền vững của CnH2n+2, phân tử của nó được biểu diễn bằng mạch thẳng và nhánh các nguyên tử cacbon C. Các chất parafin bao gồm cả khí mêtan, êtan, prôpan và các khí khác, các hợp chất với 5–17 nguyên tử C là những chất lỏng, nếu số nguyên tử C lớn hơn - là chất rắn. Các chất parafin nhẹ có khả năng bay hơi cực đại và hoà tan trong nước.
2) Nhóm các chất parafin vòng (Naftene) – các hợp chất mạch vòng bão hoà CnH2n với 5–6 nguyên tử cacbon trong một vòng (chiếm 30–60 % tổng thành phần của dầu mỏ). Hai nguyên tử cacbon trong phân tử có thể thay thế bởi các nhóm Alkin – CH2, C2H5 và các nhóm khác. Ngoài pentan và hecxan vòng, trong dầu mỏ còn gặp thấy các naften hai vòng và đa vòng. Các hợp chất này rất bền vững và ít chịu phân hủy sinh học.
3) Nhóm các chất hyđrô cacbua thơm (20–40 % tổng thành phần dầu mỏ) – các hợp chất có cấu tạo vòng không bão hoà dãy benzen, chứa ít hơn 6 nguyên tử C trong một vòng so với naftene tương ứng. Các nguyên tử cacbon trong các hợp chất này cũng có thể thay thế bằng các nhóm alkin. Trong dầu mỏ có mặt các hợp chất bay hơi với phân tử dưới dạng vòng đơn (benzen, toluol, ksilol), sau đó vòng đôi (naphtalin), vòng ba (antrapen, fenantren) và nhiều vòng (thí dụ, piren với 4 vòng).
4) Nhóm olephin (Alken) (chiếm 10 % thành phần dầu mỏ) – các hợp chất không chu kì không bão hoà với một hoặc hai nguyên tử hyđrô bên cạnh mỗi nguyên tử cacbon trong phân tử, có dạng mạch xích thẳng hay nhánh.
Tùy thuộc vị trí mỏ, dầu mỏ rất khác nhau về thành phần. Thí dụ, dầu ở Pensilvania và ở Cô Oét được phân loại là dầu nhóm parafin, dầu ở Bacu và California – nhóm naften, các loại dầu khác – thuộc các nhóm trung gian.
Trong dầu mỏ có mặt cả các hợp chất chứa lưu huỳnh (tới 7 % S), axit béo (tới 5 % O), hợp chất nitơ (tới 1% N) và một số sản phẩm thứ sinh chứa kim loại hữu cơ (với vanađi, côban, niken).
Phân tích định lượng và phân định các sản phẩm dầu trong nước biển là một nhiệm vụ khó khăn không chỉ vì chúng đa thành phần và khác biệt về hình thức tồn tại, mà còn do hệ quả nền tự nhiên của các hyđrô cacbua nguồn gốc tự nhiên và nguồn gốc sinh học. Thí dụ, gần 90 % các hyđrô cacbua phân tử thấp loại như êtilen hòa tan trong nước mặt đại dương liên quan tới hoạt động trao đổi chất của sinh vật và sự phân hủy xác của chúng. Tuy nhiên, ở những vùng bị ô nhiễm mạnh hàm lượng các hyđrô cacbua tương tự được tăng lên tới 4–5 bậc.
Theo dữ liệu khảo sát thực nghiệm, các hyđrô cacbua gốc sinh học và gốc dầu mỏ có một loạt nét khác biệt.
1) Dầu mỏ là hỗn hợp phức tạp hơn của các hyđrô cacbua với dải các cấu trúc và khối lượng phân tử tương đối rộng hơn.
2) Dầu mỏ chứa một số dãy đồng đẳng, trong đó các thành phần kế cận thường có nồng độ bằng nhau. Ví dụ, trong dãy alkan C12 – C22 tỉ lệ giữa các thành phần chẵn và lẻ bằng một, trong khi đó, hyđrô cacbua gốc sinh học trong cùng dãy này lại chứa chủ yếu là các thành phần lẻ.
3) Dầu mỏ chứa một dải rộng hơn các alkan vòng và các hyđrô cacbua thơm. Nhiều hợp chất như mono-, đi-, tri- và tetra-methylbenzen không tìm thấy trong sinh vật biển.
4) Dầu mỏ chứa rất nhiều các hyđrô cacbua naften thơm, nhiều hợp chất khác loại (trong thành phần có lưu huỳnh, nitơ, ôxy, ion kim loại), các chất dạng nhựa nhựa đường nặng – tất cả chúng thực tế không có trong sinh vật biển.
Bảng 1.3. Nguồn gốc xâm nhập hyđrô cacbua dầu mỏ vào đại dương (Tresnhicov, Smagin, 1979)
| Nguồn gốc | Triệu tấn/năm |
| Vận tải biển (không kể do hoả hoạn tầu)Hoả hoạn tầuDòng từ lục địa (kể cả nước thải đô thị)Dòng thải ven bờNguồn từ không khíMỏ dầu tự nhiênKhai thác dầu trên biển | 1,830,31,90,80,60,60,08 |
| Tổng cộng | 6,11 |
Dầu mỏ và các sản phẩm dầu là những chất ô nhiễm phổ biến nhất trong Đại Đương Thế Giới. Đến đầu những năm 80 mỗi năm khoảng 6 triệu tấn hyđrô cacbua dầu xâm nhập vào đại dương (bảng 1.3), tức 0,23 % sản lượng dầu khai thác một năm của toàn thế giới và lớn hơn nhiều so với lượng dầu thất thoát do chìm và hư hại tầu dầu trong suốt Chiến tranh Thế giới thứ hai (4 triệu tấn). Đến năm 1986 lượng dầu thất thoát đã giảm rõ rệt (bảng 1.2 và 1.3).
Các đường thâm nhập và hình thức tồn tại của các hyđrô cacbua dầu rất đa dạng (hoà tan, huyền phù, màng mỏng, dạng rắn). M. P. Nesterova (1984) ghi nhận các con đường thâm nhập sau đây:
- Thải nước rửa, nước bì và nước bẩn từ tầu biển (23 %);
- Thải tại các cảng biển và vùng nước quanh cảng, kể cả lượng thất thoát khi nạp buồng chứa của tầu (17 %);
- Các chất thải công nghiệp và nước lục địa (10 %);
- Dòng nước mưa (5 %);
- Nguồn từ sự cố tầu biển và dàn khoan trên biển (6 %);
- Khoan trên thềm lục địa (1 %);
- Nguồn từ không khí (10 %);
- Tất cả các dạng do sông tải ra (28 %).
Lượng dầu thất thoát lớn nhất liên quan tới quá trình vận chuyển chúng từ các vùng khai thác, các tình huống sự cố, xả nước rửa và nước bì từ tầu dầu, tất cả những cái đó gây nên các vết ô nhiễm thường trực dọc theo những tuyến đường hàng hải (hình 1.1).
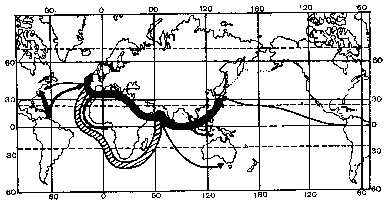
Hình 1.1. Sơ đồ các đường hàng hải chính vận chuyển dầu mỏ
Độ rộng của mũi tên tỷ lệ với khối lượng vận chuyển.
Các gạch chéo chỉ tải trọng thời kỳ từ 1967 đến 1976
Thí dụ về sự cố tầu tràn dầu lớn nhất đầu tiên có thể là vụ tai nạn của tầu chở dầu “Torri Canhiôn” năm 1967, trong các khoang chứa của nó có đến 117 nghìn tấn dầu thô Cô Oét. Gần mũi Cornuel, “Torri Canhiôn” đâm vào rạn san hô, và do bị thủng và hư hỏng 100 nghìn tấn dầu đã chảy xuống biển. Dưới tác động gió, các vết dầu lớn đã đạt tới bờ biển Cornuel, vượt qua eo biển La-Manxơ và tiến đến gần bờ Bretani (Pháp). Các hệ sinh thái biển, ven bờ và bã bị tổn thương rất lớn. Từ đó về sau, các vụ chảy dầu do sự cố tầu và dàn khoan trên biển xảy ra khá thường xuyên. Tổng cộng, trong những năm 1962–1979 gần hai triệu tấn dầu đã đi vào môi trường biển do các sự cố, trong đó từ 1962 đến 1971: 66 000 tấn mỗi năm, từ 1971 đến 1976: 116 000 tấn, từ 1976 đến 1979: 177 000 tấn (Nesterova, 1984).
Trong 30 năm gần đây, trên Đại dương Thế giới đã có gần 2000 lỗ khoan, trong đó riêng Bắc Hải bắt đầu từ năm 1962 đã khoan 1000 lỗ và 350 lỗ khoan công nghiệp. Vì rò rỉ không lớn, trên các dàn khoan mỗi năm chỉ bị mất 0,1 triệu tấn dầu, nhưng các sự cố thì không phải là ít.
Những lượng dầu lớn từ lục địa đi vào biển qua các sông cùng với nước sinh hoạt và nước mưa. Dung lượng các chất ô nhiễm do dầu từ nguồn này vượt trên 2,0 triệu tấn một năm. Dòng nước công nghiệp và nhà máy chế biến dầu hàng năm mang vào biển khoảng 0,5 triệu tấn dầu.
Số phận lượng dầu đã rơi vào biển bị quyết định bởi các quá trình sau: sự bay hơi, nhũ hóa, hoà tan, ôxy hóa, tạo thành các phức hợp dầu, lắng đọng và phân hủy sinh học (hình 1.2).
Khi xâm nhập vào biển, đầu tiên dầu lan tỏa ra dưới dạng một lớp váng trên mặt, tạo thành những vết dầu với độ dày khác nhau. Theo màu của váng dầu có thể xác định gần đúng độ dày của nó (bảng 1.4). Váng dầu làm thay đổi cường độ và thành phần phổ của ánh sáng xuyên vào môi trường nước. Các váng dầu thô chỉ cho qua 1-10 % ánh sáng (ở bước sóng 280 nm) và 60-70 % ánh sáng (ở bước sóng 400 nm). Váng dầu dày 30–40 μm hoàn toàn hấp thụ hết bức xạ hồng ngoại. Tính chất đặc trưng của dầu là phát huỳnh quang khi bị chiếu tia cực tím. Cường độ cực đại của huỳnh quang quan sát thấy ở dải sóng 440–483 nm.
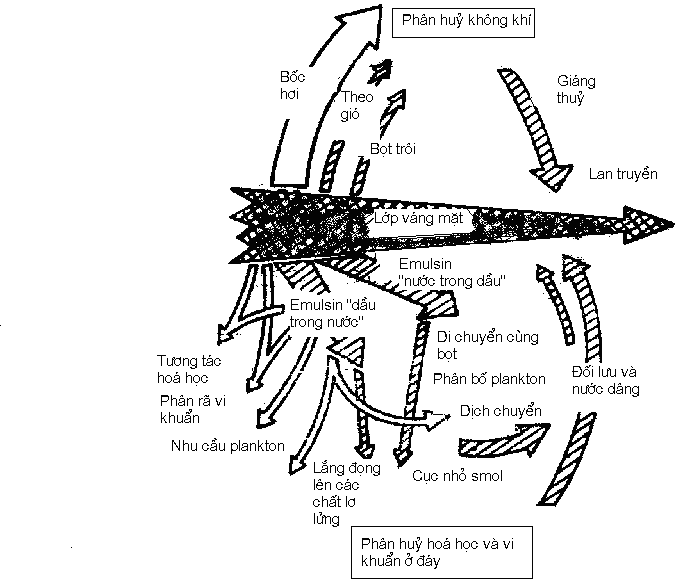
Hình 1.2. Sơ đồ tổng quát trình phân bố và phân hủy dầu tràn trên biển
(Nelson - Smit, 1977)
Sự khác biệt về các đặc trưng quang học của các váng dầu và nước biển cho phép chúng ta phát hiện từ xa và ước lượng ô nhiễm dầu trên mặt biển trong các vùng phổ cực tím, nhìn thấy và hồng ngoại. Muốn vậy, người ta ứng dụng các phương pháp thụ động và tích cực.
Các phương pháp thụ động sử dụng bức xạ tự nhiên, bị phản xạ hoặc được phát ra bởi hệ thống dầu – nước. Hiệu quả sử dụng các phương pháp này tùy thuộc vào những tính chất phát xạ và phản xạ của bề mặt, nhiệt độ, các tham số của khí quyển, dải phổ quan trắc, góc đo ngắm và phân cực.
Bảng 1.4. Một số đặc điểm váng dầu trong nước (Nelson - Smit, 1977)
| Hình dáng bề ngoài | Độ dày(μm) | Lượng dầu (l/km2) |
| Nhìn thấy | 0,038 | 44 |
| Mầu ánh bạc | 0,076 | 88 |
| Có vết màu sắc | 0,152 | 176 |
| Vân hoa màu sắc rõ | 0,305 | 352 |
| Màu sắc mờ đục | 1,016 | 1170 |
| Màu tối | 2,032 | 2340 |
Năng lượng bức xạ Mặt Trời cực tím đi tới mặt biển nằm trong dải 280–400 nm, tại đây các tính chất quang học của nước và dầu rất khác nhau: hệ số phản xạ của nước sạch là 1,5 %, của dầu thô 5–6 %, của điêzen 2–3 %. Để phát hiện váng dầu ở dải này, người ta sử dụng các hệ thống máy quét phổ, các hệ thống viđeo, những thiết bị có hệ quang học và hệ lọc tương ứng.
Khi sử dụng các loại thiết bị, bộ lọc và váng dầu khác nhau, độ tương phản tốt nhất đạt được ở vùng phổ đỏ hoặc xanh. Độ tương phản lớn nhất ứng với dải 400–630 nm, nhỏ nhất – dải 400–500 nm.
Khi quan trắc từ vệ tinh, dải 600–800 nm là dải mang nhiều thông tin nhất để phát hiện những vùng ô nhiễm của đại dương.
Tuy nhiên, nhược điểm của các quan trắc ở dải phổ nhìn thấy là sự ảnh hưởng mạnh của điều kiện khí tượng và những đặc điểm phổ của khí quyển cũng như sự độ phức tạp khi giải đoán dữ liệu quan trắc.
Các phép đo trong vùng phổ hồng ngoại dựa trên sự khác biệt nhiệt độ nước sạch và nước bị phủ váng dầu, hay sự khác biệt về các hệ số phát xạ.
Trong các phương pháp tích cực phát hiện từ xa người ta sử dụng nguồn phát xạ nhân tạo. Đó là các phương pháp định vị quang học, dựa trên sự khác biệt về hệ số phản xạ của mặt bị nhiễm bẩn và mặt nước sạch (thường là dải 300–400 và 1000–1200 nm), và các phương pháp dựa vào đo ánh sáng huỳnh quang của các váng dầu nhờ các máy dùng các bước sóng công tác 337, 354 và 530 nm.
Các phương pháp theo dõi ô nhiễm mặt nước từ xa rất có triển vọng.
Theo đánh giá gần đúng, tốc độ di chuyển các vết dầu bằng 60 % vận tốc dòng chảy và 2–4 % tốc độ gió, và dầu di chuyển theo hướng gió. Váng dầu hoàn toàn dập tắt các sóng mao dẫn, trấn áp các sóng trọng lực nhỏ và làm giảm tham số nhám gồ ghề của mặt nước đi 2–3 lần.
Lúc ban đầu tồn tại các vết dầu thì quá trình bay hơi các hyđrô cacbua có ý nghĩa lớn. Theo số liệu quan trắc, sau 12 giờ thì 25 % các hợp phần nhẹ của dầu bị bay hơi, tại nhiệt độ nước 15oC tất cả các hyđrô cacbua đến C15 bay hơi trong vòng 10 ngày (Nesterova, Nemirovskaia, 1985).
Tất cả các hyđrô cacbua có độ hoà tan yếu trong nước, và độ hòa tan càng giảm khi tăng số nguyên tử cacbon trong phân tử. Trong 1 lít nước cất hoà tan gần 10 mg các hợp chất chứa C6, 1 mg – chứa C8 và 0,001 mg chứa C12. Thí dụ, tại nhiệt độ trung bình của nước biển, độ hoà tan của benzen là 820 μg/l, toluol – 470, pentan – 360, hexsan – 138 và geptan – 52 μg/l. Các hợp phần hoà tan, trong dầu thô hàm lượng không quá 0,01 %, là những chất độc hại nhất đối với thủy sinh vật. Các chất kiểu như benzapiren cũng thuộc nhóm này.
Khi hòa trộn với nước, dầu tạo thành hai dạng nhũ tương: loại trực tiếp “dầu trong nước” và loại ngược “nước trong dầu”. Các loại nhũ tương trực tiếp, gồm các giọt dầu đường kính dưới 0,5 μm, kém bền vững và đặc biệt đặc trưng cho các loại dầu chứa các chất hoạt tính bề mặt. Sau khi tách các hợp phần bay hơi và hoà tan, dầu còn lại thường tạo thành những nhũ tương ngược nhớt, ổn định dần bởi những hợp chất cao phân tử kiểu như nhựa và nhựa đường và chứa 50–80 % nước (vữa “sôcôla”). Dưới ảnh hưởng của các quá trình phi sinh vật, độ nhớt của nhựa tăng lên và bắt đầu kết dính thành những kết hạch dầu – các hạt dầu kích thước từ 1 mm đến 10 cm (thường là 1–20 mm). Các kết hạch dầu là hỗn hợp các hyđrô cacbua phân tử cao, nhựa và nhựa đường. Lượng thất thoát dầu để hình thành các kết hạch bằng 5–10 %. Những thành tạo cấu trúc nhớt cao – “vữa sôcôla” và các kết hạch dầu, có thể duy trì trong thời gian dài trên mặt biển, bị các dòng chảy mang đi, bị tung lên bờ và lắng xuống đáy. Xung quanh các hạt kết dầu thường xuyên được Nhiều khi thủy sinh vật (tảo lam – lục và điatomê, tôm râu càng và một số động vật không xương sống khác) định cư trên các kết hạch dầu.
Thuốc bảo vệ thực vật
Các thuốc bảo vệ thực vật là nhóm lớn các chất nhân tạo dùng để chống lại những vật hại và các bệnh thực vật. Tùy thuộc mục đích sử dụng, thuốc bảo vệ thực vật chia thành các nhóm sau: thuốc diệt côn trùng – để chống côn trùng có hại, thuốc diệt nấm và diệt khuẩn – để chống nấm và các bệnh khuẩn của thực vật, thuốc diệt cỏ – chống các loại cây dại v.v... Theo tính toán của các nhà kinh tế học, mỗi đồng rúp chi để bảo vệ hóa học thực vật khỏi vật hại và bệnh, đảm bảo gìn giữ mùa màng và chất lượng các loại cây ngũ cốc, rau và về trung bình, mang lại 10 rúp, với các cây công nghiệp và cây ăn quả - tới 30 rúp. Tuy nhiên, những nghiên cứu sinh thái đã xác định rằng thuốc bảo vệ thực vật, khi tiêu diệt các vật hại mùa màng, gây tác hại to lớn đối với nhiều sinh vật có ích và làm tổn thương sự lành mạnh của các quần sinh tự nhiên. Đã từ lâu, trong nông nghiệp nổi lên vấn đề chuyển đổi phương pháp chống vật hại từ phương pháp hóa học (gây ô nhiễm môi trường) sang phương pháp sinh học (sinh thái sạch).
Hiện nay, hơn 5 triệu tấn thuốc bảo vệ thực vật được tiêu thụ trên thị trường thế giới mỗi năm. Khoảng 1,5 triệu tấn các chất này đã đi vào thành phần các hệ sinh thái đất liền và biển qua đường không khí và nước. Sản xuất thuốc bảo vệ thực vật bằng công nghiệp kèm theo xuất hiện lượng lớn các sản phẩm phụ làm ô nhiễm nước thải.
Trong môi trường nước thường gặp nhất là các đại diện của các chất diệt côn trùng, diệt nấm và diệt cỏ.
Các thuốc diệt côn trùng tổng hợp chia làm ba loại chính: hữu cơ chứa clo, hữu cơ chúa phốt pho và các cacbamat.
Thuốc diệt côn trùng hữu cơ clo sản xuất bằng phương pháp xử lý clo đối với các hyđrô cacbua thơm và hyđrô cacbua lỏng đơn vòng. Nhóm này gồm DDT (diclordifeniltricloretan) và các dẫn xuất, trong phân tử của chúng độ bền vững của các nhóm béo và nhóm thơm cùng có mặt tăng lên, tất cả các dẫn xuất chứa clo của cirlodien (eldrin, dildrin, geptaclor...) và nhiều đồng phân của hecxaclorcirclehexan (-HCCH), trong số đó nguy hiểm nhất là lindan. Những chất này có chu kỳ bán phân hủy tới vài chục năm và rất bền vững đối với phân hủy sinh học.
Trong môi trường nước thường gặp các policlorbifenil (PCB) – các dẫn xuất của DDT không có phần béo, tính được tới 210 đồng đẳng và đồng phân.
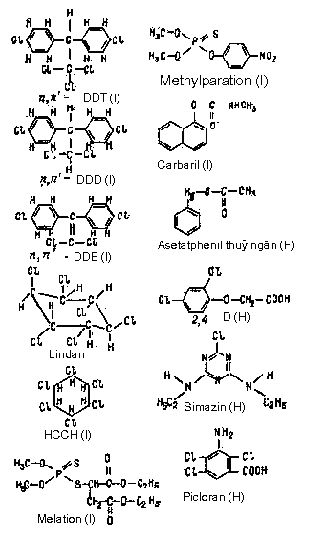
Hình 1.3. Công thức hóa học một số loại thuốc bảo vệ thực vật điển hình
I - diệt côn trùng, F - diệt nấm, khuẩn, H - diệt cỏ
Trong 40 năm gần đây, đã sử dụng 1,2 triệu tấn PCB trong sản xuất chất dẻo, thuốc nhuộm, máy biến thế, tụ điện... Các chất PCB đi vào môi trường do phát thải nước công nghiệp và đốt hủy chất thải rắn tại các bãi rác. Nguồn này đưa PCB vào khí quyển, rồi từ đó cùng với giáng thủy rơi xuống mọi vùng Trái Đất. Thật vậy, trong các mẫu tuyết lấy ở Nam Cực, hàm lượng PCB là 0,03–1,2 ng/l.
Các thuốc bảo vệ thực vật chứa phốt pho hữu cơ - đó là các ête phức tạp của các loại cồn của những axit đơn phôt pho hoặc một trong những dẫn xuất của nó thiô phôt pho. Nhóm này gồm các loại thuốc diệt côn trùng có đặc trưng tác dụng chọn lọc đối với các loại côn trùng. Đại bộ các phôt phat hữu cơ chịu phân hủy sinh hóa khá nhanh (một tháng) trong đất và nước. Người ta đã tổng hợp được hơn 50 nghìn hoạt chất, trong đó thông dụng nhất là paration, malation, fozalon, dursban.
Các chất carbamat – thường đây là các ête phức tạp của n-meta axit carbamin. Phần lớn chúng cũng có tác dụng chọn lọc.
Các chất fungicide, sử dụng để diệt bệnh nấm thực vật, trước đây có dùng muối đồng và vài khoáng chất có lưu huỳnh. Sau đó rất thông dụng dùng các chất có thủy ngân hữu cơ dạng methyl thủy ngân làm sạch bằng clo, nhưng vì sự quá độc hại của mình cho động vật được thay bằng methocsietil thủy ngân và asetat fenil mercury (thủy ngân).
Nhóm các chất herbicide gồm các sản phẩm thứ yếu axit fenocsiusus, và có tác động sinh lý mạnh. Các chất triazin (ví dụ simazin) và các chất thay thế cacbamit – u rê (monuron, diuron, picloram) nhóm lại thành nhóm mới herbicide hoà tan tốt trong nước và bền vững trong đất. Chất tác động mạnh nhất trong các chất herbicide là picloram. Để tiêu diệt toàn bộ một số dạng thực vật chỉ cần có 0,06 kg chất này trên 1 héc ta. Công thức hóa học một số chất đặc trưng pestiside trên hình 1.3.
Trong nước biển thường xuyên tìm thấy DDT và những sản phẩm phụ, PCB, HCCH, deldrin, tetraclorfenol và những hóa chất khác.
Các chất tẩy tổng hợp
Các chất tẩy thuộc nhóm lớn những chất làm giảm sức căng bề mặt của nước. Chúng có mặt trong thành phần các chất tẩy rửa tổng hợp, được dùng rộng rãi trong sinh hoạt và công nghiệp. Cùng với nước thải, các chất này xâm nhập vào nước mặt lục địa và môi trường biển. Các chất tẩy tổng hợp có chứa các poliphotphat natri, trong đó hoà tan các chất tẩy và một số hợp phần phụ độc hại cho thủy sinh vật: các chất thơm, hóa chất làm trắng (các persulphat, perborat), xô đa canxi, cacboxi-methylxeluloza, silicat natri và một số chất khác.
Phân tử của tất cả các chất tẩy được tạo thành từ các phần ưa nước và kị nước. Phần ưa nước là các nhóm: cacboxil (COO-), sunphat (OSO3-), và sunphonat (SO3-) và cả tích tụ các chất cặn với các nhóm – CH2 – CH2 – O – CH2 – CH2 – hoặc các nhóm có chứa nitơ, phôtpho. Phần kị nước thường cấu tạo từ mạch thẳng gồm 10–18 nguyên tử cacbon, hoặc mạch nhánh parafin từ các vòng benzen hay naphtalin với các chất gốc alkin.
Tuỳ thuộc bản chất và cấu trúc của phần ưa nước, các phân tử chất tẩy được phân chia thành chất hoạt tính anion mạnh (ion hữu cơ tích điện âm), hoạt tính kation mạnh (ion hữu cơ tích điện dương), lưỡng tính (biểu lộ các tính chất kation trong dung dịch axit, tính anion trong dung dịch kiềm) và không sinh ion. Các chất này không tạo thành các ion trong nước. Độ hoà tan của chúng gây nên do các nhóm chức năng có ái lực mạnh đối với nước và sự tạo thành mối liên kết hyđrô giữa các phân tử nước và các nguyên tử ôxy trong gốc polyêtilenglicôn của các chất tẩy.
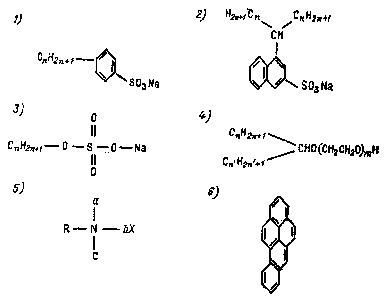
Hình 1.4. Công thức hóa học một số chất tẩy tổng hợp và benzapiren (BP)
1 - alkinbenzensulphonat (n = 518), 2 - alkilnaphtalinsulphonat (nhecali), 3 - alkilsulfat
(n = 1020), 4 - sintanol (n ≤ 16, m ≤ 10), 5 - muối amôni thứ tư, 6 - benzapiren 3,4
Phổ biến nhất trong các chất tẩy là các chất hoạt tính anion. Chúng chiếm hơn 50 % tất cả các chất tẩy sản xuất trên thế giới (ở Liên Xô tới 86 %). Phổ biến nhất là các alkilaril-sulphonat (sulphonol) và alkinsulphat. Các phân tử sulphonol có chứa vòng thơm, trong đó các nguyên tử hyđrô được thay thế bằng một hay vài nhóm alkin, còn phần dư của axit sulphuric đóng vai trò chất dính nước. Nhiều chất alkinbenzolsulphonat và alkilnaphtalinsulphonat (hình 1.4) thường được sử dụng trong sản xuất các chất tẩy rửa sinh hoạt và công nghiệp.
Các alkilsulphat (hình 1.4) được sản xuất dựa trên các cồn béo. Trong các chất alkilsulphat nguyên sinh, nhóm sulphoeste nằm ở cuối phân tử. Trong các chất alkilsulphat thứ sinh, nó liên kết với một trong các nguyên tử cacbon nằm bên trong phân tử.
Các chất tẩy không sinh ion là những sản phẩm cao phân tử trùng ngưng ôxit êtilen hoặc propilen với các hợp chất chứa nguyên tử hyđrô di động, thí dụ cồn béo, axit cacbolic, alkinphenol, phenol. Thí dụ, các sintanol (xem hình 1.4) – các ête poliethylen trên cơ sở các cồn thứ sinh, được phân biệt với nhau bằng hàm lượng ôxit ethylen. Ở Liên Xô, về khối lượng sản xuất, các chất tẩy không sinh ion chiếm 11–16 % tổng lượng và thường được sử dụng cho các mục đích công nghiệp (OP–7, OP–10, các sintanol, sintamid, proxsanol và các chất khác).
Các muối nhóm bốn thuộc loại các chất tẩy hoạt tính kation. Thí dụ như các muối amôni (xem hình 1.4), chứa gốc alkin với mạch thẳng từ 12–18 nguyên tử cacbon, sau đó nhóm methyl, ethyl hoặc benzin (a, b, c) và nguyên tử halogen hoặc phần dư methyl– hay ethylsulphat (x). Tỉ phần các chất hoạt tính kation là 1–2,5 % tổng sản lượng các chất tẩy.
Các chất tẩy lưỡng tính hiện mới chỉ sản xuất những loạt thử nghiệm và chưa dùng rộng trong kinh tế quốc dân.
Sự có mặt các chất tẩy trong nước thải công nghiệp là do chúng được dùng trong các quá trình như làm giầu tách đãi quặng, tách sản phẩm trong công nghệ hóa học, sản xuất các polime, cải thiện điều kiện khoan ở các lỗ khoan dầu và khí, chống ăn mòn thiết bị.
Trong nông nghiệp, các chất tẩy được dùng trong thành phần của thuốc bảo vệ thực vật. Nhờ các chất hoạt hóa mặt, người ta nhũ hóa được các chất độc dạng lỏng hoặc dạng bột, không hoà tan trong nước, nhưng hòa tan trong các chất hòa tan hữu cơ. Ngoài ra, nhiều chất tẩy bản thân chúng có các tính chất diệt côn trùng và diệt cỏ.
Các hợp chất có thuộc tính gây ung thư
Các chất gây ung thư – đó là các hợp chất đồng loại hóa học, biểu hiện hoạt tính biến dạng và có khả năng gây nên những biến đổi gây ung thư, sinh quái thai (làm rối loạn quá trình phát triển phôi), hay biến đổi đột biến trong cơ thể. Tùy thuộc các điều kiện tác động, chúng có thể dẫn đến sự kìm hãm tăng trưởng, đẩy nhanh quá trình già, phát sinh độc tố, phá hủy sự phát triển cá thể và làm biến đổi quỹ gien sinh vật.
Thuộc loại các chất có đặc tính gây ung thư có: các hyđrô cacbua béo chứa clo với mạch ngắn các nguyên tử cacbon trong phân tử, vinylclorit, thuốc bảo vệ thực vật và đặc biệt hyđrô cacbua thơm đa vòng (PAH). Đó là các hợp chất hữu cơ đa phân tử, trong phân tử của chúng vòng benzen là yếu tố cấu chúc chính. Các chất PAH không thay thế chứa trong phân tử từ 3 đến 7 vòng benzen, liên kết với nhau theo nhiều kiểu. Còn một số lượng lớn các cấu trúc đa vòng, có chứa nhóm chức năng hoặc trong vòng benzen, hoặc trong mạch bên. Đó là halogen-, amino-, sulpho-, nitro- và các loại cồn, anđehit, ête, ketone, axit, quinon, các hợp chất khác có mạch thơm.
Độ hoà tan của PAH trong nước không lớn và giảm dần với sự tăng khối lượng phân tử: từ 16 100 μg/kg (acenaphtilen) đến 0,11 μg/l (3,4-benzapiren). Sự có mặt các muối trong nước thực tế không ảnh hưởng đến sự hoà tan của PAH. Nhưng với sự có mặt của benzol, dầu, sản phẩm dầu, chất tẩy và các chất hữu cơ khác, thì độ hoà tan của PAH tăng lên rất mạnh. Trong nhóm PAH không thay thế, trong điều kiện thiên nhiên được biết đến nhiều nhất và thông dụng hơn cả là 3,4-benzapiren (BP) (xem hình 1.4).
Những nguồn PAH trong môi trường có thể là các quá trình tự nhiên và nhân sinh. Nồng độ của BP trong tro núi lửa là 0,3–0,9 μg/kg. Điều này có nghĩa là cùng với tàn tro, mỗi năm 1,2–24 tấn BP có thể đi vào môi trường. Vì vậy, lượng PAH cực đại trong trầm tích hiện đại của đáy Đại dương Thế giới (hơn 100 μg/kg chất khô) được phát hiện ở các vùng hoạt động kiến tạo mạnh, do tác động nhiệt của lòng đất.
Theo thông tin hiện có, một số thực vật và động vật biển có thể tổng hợp PAH. Trong tảo và cỏ biển gần vùng bờ tây Trung Mỹ, lượng BP đạt tới 0,44 μg/g, trong một số loài tôm ở Bắc Băng Dương – 0,23 μg/g. Các vi khuẩn kị khí tạo ra đến 8,0 μg BP từ 1 g các chất chiết suất lipit của plankton. Mặt khác, có những dạng vi khuẩn đặc biệt ở biển và trong đất phân hủy được các hyđrô cacbua, kể cả PAH.
Theo đánh giá của L. M. Sabad (1973) và A. P. Ilnhiski (1975), mật độ nền BP được tạo thành trong khi tổng hợp BP bởi thực vật và hoạt động núi lửa, bao gồm: trong đất: 5–10 μg/kg (chất khô), trong thực vật: 1–5 μg/kg, trong nước của các thủy vực nước ngọt: 0,0001 μg/l. Tương ứng với những nồng độ đó, người ta đã đưa ra những cấp độ ô nhiễm của các đối tượng trong môi trường (hình 1.5).
Các nguồn nhân sinh chủ yếu của PAH trong môi trường - đó là sự nhiệt phân các chất hữu cơ trong quá trình đốt cháy các nguyên liệu, gỗ và nhiên liệu. Sự tạo thành PAH bằng nhiệt phân xảy ra khi đạt nhiệt độ 650–900 oC và thiếu hụt ôxy trong ngọn lửa. Người ta thấy BP được được tạo thành nhiều nhất trong quá trình nhiệt phân củi gỗ với nhiệt độ 300–350 oC (Dikun, 1970).
Theo ước lượng của M. Ziussa (1976), phát thải BP toàn cầu trong các năm 70 bằng khoảng 5 000 tấn một năm, trong đó có 72 % từ công nghiệp và 27 % – từ tất cả các dạng cháy khác.
Bảng 1.5. Mức ô nhiễm benzapiren (BP) của môi trường xung quanh
(Ilnhiski, 1975)
| Đối tượng | ||||
| Mức độ ô nhiễm, μg/kg | ||||
| Yếu | Đáng kể | Mạnh | ||
| Đất | 20 – 30 | 31 – 100 | > 100 | |
| Thực vật | ≤ 10 | 11 – 20 | > 20 | |
| Nước (μg/l) | ≤ 0,005 | ≤ 0,01 | > 0,01 | |
| Trầm tích đáy (cát) | 20 – 30 | ≤ 100 | > 100 | |
| Thủy thực vật bậc cao | 15 – 20 | ≤ 50 | > 50 |
Kim loại nặng
Các kim loại nặng (thủy ngân, chì, cađimi, kẽm, đồng, asen...) thuộc số các chất ô nhiễm phổ biến và cực kì độc. Chúng được dùng rộng rãi trong nhiều ngành công nghiệp, vì vậy, mặc dù có các biện pháp làm sạch, hàm lượng hợp chất chứa các kim loại nặng trong nước thải công nghiệp tương đối lớn. Khối lượng lớn các hợp chất này đi vào đại dương qua khí quyển. Các dòng của một số kim loại nguồn gốc địa hóa và nguồn gốc công nghiệp được so sánh trong bảng 1.6. Với các quần thể sinh vật biển, thì nguy hiểm nhất là thủy ngân, chì và cađimi.
Thủy ngân được mang tới đại dương từ lục địa và từ khí quyển. Khi phong hóa các đá trầm tích và phun trào, hàng năm xuất ra 3,5 tấn thủy ngân. Trong thành phần bụi không khí có chứa gần 12 000 tấn thủy ngân, và phần lớn có nguồn gốc nhân sinh. Trong quá trình phun núi lửa và cùng với giáng thủy khí quyển, mỗi năm 50 nghìn tấn thủy ngân đ xuống mặt đại dương, còn trong quá trình khử khí của thạch quyển - 25–150 nghìn tấn. Gần nửa sản lượng công nghiệp năm của kim loại này (9–10 nghìn tấn) bằng những con đường khác đi vào đại dương. Hàm lượng thủy ngân trong than đá và dầu mỏ trung bình bằng 1 mg/kg, vì vậy, do đốt nhiên liệu khoáng, Đại dương Thế giới nhận hơn 2 nghìn tấn/năm. Sản lượng khai thác năm của thủy ngân vượt 0,1 % tổng hàm lượng của nó trong Đại dương Thế giới, nhưng nhập lượng nhân tạo đã vượt trội lượng mang ra bởi sông, điều này là đặc trưng cho nhiều kim loại (bảng 1.7).
Bảng 1.6. Dòng các kim loại nguồn địa hóa và công nghiệp (Gerlach, 1985)
| Nguồn gốc | Đơn vị | Pb | Hg | Cd | Sb | Cr | Se | As | Cu | Zn |
| Vỏ trái đất | mg/kg | 15 | 0,06 | 0,2 | 0,2 | ? | 0,09 | 2 | 45 | 40 |
| Nước đại dương | μg/l | 0,002 | 0,007 | 0,1 | 0,3 | 0,3 | 0,5 | 2 | 2 | 3 |
| Toàn bộ ĐDTG | 106 t | 2,8 | 10 | 140 | 420 | 420 | 700 | 2800 | 2800 | 4200 |
| Xói lở | 103 t/năm | 150 | 3,5 | 0,5 | 1,3 | 236 | 7,2 | 72 | 325 | 720 |
| Đốt nhiên liệu | 103 t/năm | 34 | 2,0 | 0,2 | ? | 1,5 | 1,1 | 8,2 | 2,1 | 37 |
| Khai thác | 103 t/năm | 3500 | 9,0 | 15 | 70 | 3000 | 1,2 | 30 | 7500 | 5000 |
| Sản lượng năm | % hàm lượng trong ĐDTG | 125 | 0,1 | 0,01 | 0,015 | 0,7 | 2.10-4 | 10-4 | 0,3 | 0,1 |
Hàm lượng thủy ngân trong nước đại dương không vượt ra khỏi giới hạn 5–15 ng/l. Trong nước biển nó có mặt trong các dạng sau (Brosse, 1985): (65,8 %), (12,3 %), (12 %), (4,3 %), (3 %), (1,1 %), (0,2 %). Ba dạng sau cùng thuộc dạng bay hơi.
Ở những vùng ô nhiễm bởi nước thải công nghiệp, nồng độ thủy ngân trong dung dịch và trong chất lơ lửng tăng mạnh. Ở đây, vi khuẩn đáy chuyển hóa các clorit thành thủy ngân mêtil (đơn và đôi) CH3Hg độc tính cao. Sự nhiễm độc hải sản đã nhiều lần làm cho dân cư ven biển bị nhiễm độc thủy ngân. Tính đến năm 1977, ở Nhật đã có tới 2800 nận nhân của bệnh Minamata. Nguyên nhân của bệnh này là do các chất thải của các xí nghiệp chế clovinhil và axetanđehit, ở đó thủy ngân clorit được dùng làm chất xúc tác. Nước thải làm sạch chưa tốt đã đi vào vịnh Minamata.
Bảng 1.7. Dòng các kim loại (103 tấn/năm) tạo bởi các quá trình tự nhiên
và nhân tạo (Valđichuc, 1977)
| Nguyên tố | Nguồn nước sông tự nhiên | Các nguồn nhân tạo |
| Sắt (Fe) | 25000 | 319000 |
| Mangan (Mn) | 440 | 1600 |
| Đồng (Cu) | 375 | 4460 |
| Kẽm (Zn) | 370 | 3930 |
| Niken (Ni) | 300 | 358 |
| Chì (Pb) | 180 | 2330 |
| Molibđen (Mo) | 13 | 57 |
| Bạc (Ag) | 5 | 7 |
| Thủy ngân (Hg) | 3 | 7 |
| Thiếc (Sn) | 1,5 | 166 |
| Ăngtimoan (Sb) | 1,3 | 40 |
Chì – nguyên tố phân tán tiêu biểu, chứa trong tất cả các hợp phần môi trường: trong đá, đất mầu, nước thiên nhiên, khí quyển, sinh vật. Cuối cùng, chì phát tán mạnh vào môi trường trong quá trình hoạt động sản xuất của con người. Đó là phát thải cùng với nước thải công nghiệp và sinh hoạt, khói và bụi của các nhà máy, khí xả của động cơ đốt trong.
Theo những ước lượng của V. V. Đobrovolski (1987), sự tái phân bố khối lượng chì giữa lục địa và Đại dương Thế giới như sau. Với dòng nước sông, nồng độ chì trong nước trung bình 1 μg/l, lượng chì hòa tan trong nước mang vào đại dương là gần tấn/năm, ở pha rắn của các chất lơ lửng của sông khoảng tấn/năm, trong đetrit hữu cơ vụn tinh - tấn/năm. Nếu tính rằng, trong dải hẹp ven bờ ở thềm lục địa, hơn 90 % chất lơ lửng sông bị lắng đọng và phần lớn các hợp chất hoà tan của các kim loại bị hấp thụ bởi các keo ôxit sắt, thì kết cục, vùng thẳm đại dương chỉ còn nhận được khoảng tấn từ chất lơ lửng hạt mịn và tấn hợp chất hòa tan.
Dòng chì di cư từ các lục địa vào đại dương không chỉ có theo nước sông, mà còn qua khí quyển. Với bụi khí lục địa, đại dương nhận tấn chì một năm. Nguồn chì gia nhập từ giáng thủy được đánh giá vào khoảng tấn/năm với nồng độ chì trong nước mưa 1–6 μg/l. Những nguồn chì đi vào khí quyển là phát thải núi lửa (15–30 tấn/năm từ các sản phẩm phún trào mịn và tấn/năm từ các hạt dưới micromet), các hợp chất hữu cơ nhẹ từ thảm thực vật (250–300 tấn/năm), sản phẩm từ các vụ cháy ( tấn/năm) và công nghiệp hiện đại. Sản lượng chì tăng từ tấn/năm vào đầu thế kỷ 19 lên tấn/năm đầu những năm 80 thế kỷ 20. Lượng phát thải chì hiện nay vào môi trường từ các nguồn công nghiệp và sinh hoạt được ước lượng khoảng tấn/năm.
Cađimi, với sản lượng toàn thế giới ở những năm 70 đã đạt tấn/năm, cũng đi vào đại dương cùng với dòng nước sông và qua khí quyển. Theo một số đánh giá, lượng cađimi qua không khí bằng tấn/năm.
Sự đổ phế thải xuống biển nhằm mục đích chôn giữ
Nhiều nước ven biển thực hiện chôn cất trong biển các vật liệu và các chất, chẳng hạn như bùn cát từ công trình nạo vét đáy, cặn lỗ khoan, chất thải công nghiệp, rác xây dựng, chất thải rắn, chất nổ và hóa chất, chất thải phóng xạ và những chất khác. Lượng chôn cất bằng gần 10 % tổng lượng các chất ô nhiễm thâm nhập vào Đại dương Thế giới. Thật vậy, từ năm 1976 đến 1980, mỗi năm với mục đích chôn thải người ta đã đổ hơn 150 triệu tấn các loại chất thải vào biển.
Căn cứ để chôn thải trong biển là khả năng của môi trường biển có thể tái chế được một lượng lớn các chất hữu cơ và vô cơ mà không có hại gì đặc biệt đối với chất lượng nước. Tuy nhiên, khả năng này không phải vô hạn. Vì vậy, chôn thải được xem như một giải pháp bất đắc dĩ, sự nhượng bộ tạm thời của xã hội trước sự bất cập của công nghệ. Từ đây, vấn đề đề xuất và luận chứng khoa học cho các phương pháp điều chỉnh đổ thải xuống biển có tầm quan trọng đặc biệt.
Trong rác thải sản xuất công nghiệp có mặt những chất hữu cơ và hợp chất kim loại nặng khác nhau. Rác sinh hoạt trung bình chứa (trên khối lượng chất khô) 32–40 % các chất hữu cơ, 0,56 % nitơ, 0,44 % phôtpho, 0,155 % kẽm, 0,085 % chì, 0,001 % cađimi, 0,001 % thủy ngân. Chất cặn của nhà máy làm sạch nước sinh hoạt chứa (trên khối lượng chất khô) đến 12 % các chất mùn, 3 % nitơ tổng, 3,8 % phôtpho, 9–13 % chất béo, 7–10 % các chất đường và bị ô nhiễm bởi các kim loại nặng. Các vật liệu nạo vét đáy cũng có thành phần tương tự như vậy.
Trong thời gian đổ thải, khi vật liệu đi qua cột nước thì một phần các chất ô nhiễm chuyển vào dung dịch, làm thay đổi chất lượng nước, một phần khác bị các hạt lơ lửng hấp phụ và chuyển vào trầm tích đáy. Đồng thời độ đục nước tăng lên. Sự hiện diện các chất hữu cơ thường dẫn đến tiêu hao nhanh ôxy trong nước và không hiếm khi dẫn tới chỗ hoàn toàn triệt tiêu ôxy, sự hoà tan các chất lơ lửng, tích tụ các kim loại ở dạng tan, xuất hiện hyđrô sunphua. Sự có mặt lượng lớn các chất hữu cơ sẽ tạo ra trong bùn đáy một môi trường khử bền vững, trong đó xuất hiện một loại nước bùn đặc biệt, chứa hyđrô sunphua, amiac, các ion kim loại ở dạng khử. Trong đó xảy ra quá trình khử các sunphat và nitrat, tạo ra các phôtphat.
Các vật liệu thải có tác động khác nhau tới các cơ thể sinh vật nổi, sinh vật bơi trong nước và sinh vật đáy. Trong trường hợp tạo thành váng mặt chứa các hyđrô cacbua dầu và các chất tẩy, chế độ trao đổi khí tại biên không khí – nước bị phá hoại. Điều đó dẫn đến làm chết ấu trùng các động vật không xương sống, chứng cá và cá bột, kích thích tăng trưởng số lượng vi sinh vật ôxy hóa dầu và sinh vật gây mầm bệnh. Sự hiện diện chất lơ lửng ô nhiễm trong nước làm xấu điều kiện dinh dưỡng, hô hấp và trao đổi chất của nhiều thủy sinh vật khác, làm giảm tốc độ tăng trưởng, cản trở sự trưởng thành sinh dục của động vật phù du giáp xác. Các chất ô nhiễm thâm nhập vào dung dịch, có thể tích lũy trong mô và các bộ phận của thủy sinh vật và tác động độc hại tới chúng. Chôn thả các nguyên liệu xuống đáy và độ đục nước đáy tăng cao trong thời gian dài sẽ làm chết ngạt các dạng sinh vật bám đáy di chuyển chậm. Với các loài cá, thân mềm và giáp xác sống sót thì tốc độ tăng trưởng bị giảm do điều kiện thức ăn và hô hấp sút kém. Không hiếm khi thành phần loài của quần thể đáy bị biến đổi.
Trong khi tổ chức hệ thống kiểm soát đổ thải vào biển, việc xác định các vùng đổ thải có tính đến các tính chất của vật liệu và các đặc trưng của nước biển có ý nghĩa quyết định. “Hiệp định về phòng chống ô nhiễm biển do đổ thải và các nguyên liệu khác” (hiệp định Luân đôn về chôn thải, năm 1972) có chứa những tiêu chí cần thiết để giải quyết vấn đề. Những yêu cầu chính của Hiệp định như sau:
1) Đánh giá số lượng, trạng thái và tính chất (lý học, hóa học, sinh hóa, sinh học) của các vật liệu vứt bỏ, độc tính của chúng, độ bền vững, xu thế tích lũy và biến đổi sinh học trong môi trường nước và trong các sinh vật biển.
2) Sử dụng những khả năng vô hiệu hóa, làm mất tác hại và tái tận dụng các chất thải.
3) Chọn các vùng đổ thải có tính đến những yêu cầu làm loãng tối đa các chất, giảm thiểu sự lan truyền của chúng ra ngoài vùng đổ thải, kết hợp thuận lợi các điều kiện thủy văn và thủy lý.
4) Đảm bảo cách ly những vùng đổ thải xa các vùng vỗ béo và đẻ trứng của cá, xa nơi sinh sống của các loài thủy sinh vật quý hiếm và nhạy cảm, xa các vùng nghỉ dưỡng và các vùng kinh tế.
Để đánh giá định lượng về tình trạng ô nhiễm hóa học môi trường những vùng đổ thải, xác định động thái các mức ô nhiễm nước biển và trầm tích đáy và định ra khối lượng thải cho phép vào biển, cần phải tiến hành tính cân bằng đối với tất cả các chất ô nhiễm trong thành phần vật liệu thải (Slưghin, 1983).
Các đồng vị phóng xạ nguồn gốc kĩ nghệ
Đại dương vốn có độ phóng xạ tự nhiên, vì trong đại dương có 40K, 87Rb, 3H, 14C và các đồng vị phóng xạ của các chỗi uran và thori. Hơn 90 % độ phóng xạ tự nhiên của nước đại dương là do 40K, tức bằng 18,5.1021 Bk. Đơn vị độ phóng xạ trong hệ SI – bekkelium (Bk), bằng phóng xạ của một đồng vị, trong 1 s diễn ra một động tác phân rã. Trước đây, người ta đã sử dụng đơn vị độ phóng xạ ngoài hệ thống curi (Cu), tương đương độ phóng xạ của một đồng vị, trong 1 s diễn ra 3,7.1010 động tác phân rã.
Các chất phóng xạ nguồn gốc kỹ nghệ, chủ yếu là những sản phẩm phân tách uran và plutoni, bắt đầu xâm nhập vào đại dương với lượng lớn từ sau năm 1945, tức từ khi bắt đầu các vụ thử vũ khí hạt nhân và phát triển mạnh sản xuất công nghiệp các vật liệu phân chia và các đồng vị phóng xạ. Người ta phân ra ba nhóm nguồn: 1) thử vũ khí hạt nhân, 2) đổ thải chất thải phóng xạ, 3) sự cố tầu có động cơ nguyên tử và sự cố liên quan tới việc sử dụng, vận chuyển và sản xuất các đồng vị phóng xạ.
Thành phần các đồng vị nhân tạo đi vào đại dương được xác định chủ yếu bằng những sản phẩm phân chia nhiên liệu hạt nhân (bảng 1.8). Tương quan giữa chúng có thể thay đổi tuỳ theo dạng nhiên liệu, tốc độ và các điều kiện diễn ra phản ứng.
Bảng 1.8. Những đồng vị phóng xạ quan trọng nhất trong nước biển
(Khardi và nnk., 1973; Rais, 1971)
| Tên đồng vị | Chu kỳ phân rã | Dạng phát xạ | Tên đồng vị | Chu kỳ phân rã | Dạng phát xạ |
| Các đồng vị thiên nhiên | Các nguyên tố chuyển hóa uran | ||||
| Triti 3H | 12,3năm | β | Pu – 238 | 86 năm | α |
| Cacbon –14 | 5760 năm | β | Pu – 239 | 24400 năm | α |
| Kali – 40 | 1,3.109 năm | β | Pu – 240 | 6660 năm | α |
| Rb – 87 | 4,7.1010 năm | β | Pu – 241 | 13,2 năm | α |
| Po – 210 | 0,38 năm | α | Am – 241 | 458 năm | α – |
| U – 234 | 2,5.105 năm | α | Sản phẩm phân tách trong lò hạt nhân | ||
| U – 235 | 7,1.108 năm | α | Ba – 140 | 12,8 ngày | β – |
| U – 238 | 4,5.109 năm | α | Kr – 85 | 10,6 năm | β |
| Sản phẩm kích hoạt | Sr – 89 | 0,14 năm | β | ||
| P – 32 | 0,04 năm | β | Sr – 90 | 28 năm | β |
| Cr – 51 | 0,08 năm | K – | Y – 90 | 2,5 ngày | β |
| Mn – 54 | 0,86 năm | K – | Y – 91 | 0,16 năm | β |
| Fe – 55 | 2,7 năm | K | Nb – 95 | 0,10 năm | β – |
| Co – 57 | 0,74 năm | K – | Zr – 95 | 0,18 năm | β – |
| Co – 60 | 5,3 năm | β – | Ru – 103 | 0,11 năm | β – |
| Zn – 65 | 0,67 năm | K – | Ru – 106 | 1 năm | β – |
| Ag – 110 | 0,69 năm | β – | I – 131 | 7,3 ngày | β – |
| Cs – 134 | 2,1 năm | β – | Cs – 137 | 30 năm | β |
| Ce – 35 | 0,239 năm | β | Ce – 144 | 0,78 năm | β – |
| Ca – 45 | 0,438 năm | β | Ar – 41 | 2 giờ | β |
| Na – 24 | 15 giờ | β – | Xe – 133 | 5 ngày | β |
Ghi chú: K – bức xạ Rơngen K.
Trong giai đoạn 1948–1962 đã thực hiện gần 450 vụ nổ bom nguyên tử, theo công suất của chúng có thể đánh giá gần đúng số lượng đồng vị phóng xạ (đối với các dạng cực kỳ nguy hiểm 90Sr và 137Cs – bảng 1.9), xuất hiện trong khí quyển ở dạng các sôn khí. Tổng lượng 137Cs, đi vào lớp bình lưu vào đầu năm 1981, theo đánh giá của A. A. Moisev (1985), bằng 96.1016 Bk. Nếu chấp nhận tỷ lệ độ phóng xạ 137Cs/90Sr bằng 1,6, thì lượng tương ứng của 90Sr tỏa ra sẽ là 60.1016 Bk.
Bụi và sôn khí phóng xạ trong quá trình hoàn lưu của các khối không khí lan ra những lãnh thổ rộng và rơi xuống mặt Trái Đất chủ yếu trong đới 45o N – 45o S, hơn nữa phần lớn mưa phóng xạ rơi ở bắc bán cầu. Nhiều đồng vị phóng xạ với chu kỳ bán phân rã ngắn, mặc dù cũng được phát hiện sau vụ nổ trong nước và trong nhiều sinh vật biển, trong các đợt mưa phóng xạ toàn cầu hầu như không gặp thấy. Trước hết ở đây có mặt 90Sr và 137Cs với chu kỳ bán phân rã khoảng 30 năm.
Đồng vị phóng xạ nguy hiểm nhất từ những mảnh vụn của các đầu đạn hạt nhân không chưa phản ứng hết là 239Pu (T1/2=24,4.103 năm), rất độc như một chất hóa học. Theo mức độ phân hủy các sản phẩm phân tách 90Sr và 137Cs, nó trở thành một hợp phần ô nhiễm chính. Tới thời điểm “tạm hoãn” thử vũ khí hạt nhân trong khí quyển (năm 1963), độ phóng xạ 239Pu trong môi trường bằng 2,5.1016 Bk. Tới năm 1972, khoảng một nửa lượng này đã rơi ở những khu vực thử.
Các chất 3H, 24Na, 65Zn, 59Fe, 14C, 31Si, 35S, 45Ca, 54Mn, 57,60Co và các chất khác, xuất hiện trong khi tương tác của các nơtron với các yếu tố cấu trúc và môi trường bên ngoài, tạo thành một nhóm riêng các đồng vị phóng xạ. Những sản phẩm chính của các phản ứng hạt nhân với nơtron trong môi trường biển là các đồng vị phóng xạ của natri, kali, phôtpho, clo, brôm, canxi, mangan, lưu huỳnh, kẽm, bắt nguồn từ những nguyên tố hòa tan trong nước biển. Đây là độ phóng xạ liên hệ.
Bảng 1.9. Lượng 90Sr và 137Cs tạo thành trong các vụ thử vũ khí hạt nhân
trong khí quyển (theo các báo cáo của Uỷ ban LHQ về bức xạ nguyên tử)
| Năm thử nghiệm | Tổng công suấtcác vụ nổ, Mt* | |||
| Lượng tính toán, 1016 Bk | ||||
| 90Sr | 137Cs | |||
| 1945 – 1951 | 0,02 | 0,0075 | 0,0127 | |
| 1952 – 1954 | 1,0 | 0,37 | 0,646 | |
| 1955 – 1956 | 5,6 | 2,1 | 3,55 | |
| 1957 – 1958 | 31,0 | 11,7 | 19,7 | |
| 1859 – 1960 | – | – | – | |
| 1961 – 1962 | 101 | 38,0 | 64,5 | |
| Tổng cộng | 138,62 | 52,18 | 88,41 |
Phần lớn các đồng vị phóng xạ, đi vào môi trường biển, có các đồng loại của mình có mặt thường trực như 239Pu, 239Np, 99Tc, các chất chuyển hóa Pluton không đặc trưng đối với thành phần nước biển, và các vật thể sống của đại dương cần phải thích nghi lại lần nữa với chúng.
Kết quả chế biến nhiên liệu hạt nhân làm xuất hiện một lượng đáng kể chất thải phóng xạ ở dạng lỏng, rắn và khí. Khối lượng chất thải chủ yếu là các dung dịch phóng xạ. Vì tính đến giá thành cao của quá trình chế biến và bảo quản chất cô đặc ở những bể chứa chuyên dụng, nên một số quốc gia chọn cách đổ các chất thải vào đại dương theo dòng nước sông hoặc chứa chúng trong các thùng bê tông và thả xuống đáy các rãnh sâu đại dương. Với các đồng vị phóng xạ Ar, Xe, Cm, Th vẫn chưa có những phương pháp cô đặc hữu hiệu, vì vậy chúng có thể nhập vào đại dương cùng với giáng thủy và nước thải. Từ năm 1944 đến 1971, nhà máy sản xuất pluton trên sông Columbia (Mỹ) hàng tháng đã đổ 92,5.1013 Bk các chất khác phóng xạ (gần 60 chất), trong đó có 65Zn và 51Cr có hoạt tính sinh học. Từ năm 1969 đến 1976 tổng thải 137Cs xuống biển Ailen là 18,5.1015 Bk, còn 134Cs – 3,5.1015 Bk. Những lần đổ thải tương tự thường là nguyên nhân làm cho mức phóng xạ nền ở các vùng rộng lớn của đại dương vượt trên mức nền rất nhiều.
Chôn thải dưới đáy đại dương như một phương pháp loại bỏ các chất thải phóng xạ đã được dùng rộng rãi trong những thập niên gần đây. Từ năm 1946 đến 1970, Uỷ ban năng lượng hạt nhân Hoa Kì đồng ý cho chôn thải với độ phóng xạ 0,52.1015 Bk ở Thái Bình Dương và với độ phóng xạ 3,0.1015 Bk ở Đại Tây Dương. Từ năm 1967 đến 1976, tám nước thành viên Tổ chức hợp tác kinh tế châu Âu đã chôn xuống Bắc Đại Tây Dương 45970 tấn chất thải với tổng độ phóng xạ 0,17.1015Bk. Người ta đang cố gắng tiến hành chôn vùi các công tơ nơ chất thải dưới các vỉa địa chất đáy ở vũng sâu đại dương hoặc trong những thành tạo địa chất thích hợp của thạch quyển trên lục địa.
Khi khai thác các hệ thống năng lượng nguyên tử trên các tầu hay tầu ngầm (ước tính đã có tới vài trăm chiếc), hàng năm đang đưa vào biển gần 3,7.1016 Bk cùng với cặn thải có trao đổi iôn, gần 18,5.1013 Bk cùng với các chất thải lỏng và 12,6.1013 Bk do rò rỉ. Những tình huống sự cố cũng góp phần đáng kể vào độ phóng xạ đại dương. Thí dụ, năm 1963 sau khi chìm tầu ngầm “Treser”, tại đáy Đại Tây Dương độ phóng xạ đã trở nên cao hơn 1016 Bk.
Đến nay, tổng lượng phóng xạ do con người mang vào đại dương chưa vượt quá 5,5.1019 Bk, vẫn chưa nhiều so với mức tự nhiên (18,5.1021 Bk). Tuy nhiên, tính tập trung và phân bố không đều các chất phóng xạ tạo nên mối nguy hiểm nhiễm xạ nước và thủy sinh vật ở một số vùng riêng biệt của đại dương.